Metall und Legierungsstoff im Portrait
Die Weiterverarbeitung von Eisen zu Stahl wäre ohne eine ganze Reihe weiterer Elemente kaum denkbar. Erst sie machen aus einer simplen Eisen-Kohlenstoff-Verbindung einen enorm vielfältigen, hochpräzise auf zahlreiche Anwendungen abstimmbaren modernen Werkstoff. Das Element Nickel spielt hierbei eine besonders herausragende Rolle. Ein Großteil der weltweiten Nickelproduktion wird in Stahlwerken verwendet, um dort die unterschiedlichsten Endprodukte zu veredeln.
Nickel: Die grundlegenden Fakten
Ähnlich, wie viele andere Legierungselemente, befindet sich Nickel auf der Periodentafel nicht weit vom Eisen entfernt. Mit der Ordnungszahl 28 ist es sogar ein Nachbar des Eisens (26).
| Nickel | |
|---|---|
| Name, Symbol, Ordnungszahl | Nickel / Ni / 28 |
| Elementkategorie | Übergangsmetalle |
| Aussehen | silbrig metallisch glänzend |
| Masseanteil an der Erdhülle | 0,015 % |
| Aggregatzustand | fest |
| Kristallstruktur | kubisch flächenzentriert |
| Atommasse | 58,6934 u |
| Härte nach Mohs | 4,0 |
| Schmelzpunkt | 1.455° C |
| Siedepunkt | 2.730° C |
Der internationale Name des Nickels führt auf eine Gruppe von Berggeistern zurück: die sogenannten Nickel. Er rührt daher, dass Bergleute im Mittelalter Nickel hauptsächlich in Form des (heute so bezeichneten) Minerals Nickelin fanden – ein Nickelarsenid, auch bekannt als Rotnickelkies.
Dieses Mineral sieht Kupfererz zum Verwechseln ähnlich. Da es jedoch kein Kupfer enthält und die danach suchenden Bergleute es dementsprechend nicht aus dem Nickelin extrahieren konnten, glaubten sie, es sei von den Nickeln verhext worden. Sie nannten es deshalb Kupfernickel.
Zwar war Nickel daher bereits durch den mittelalterlichen Bergbau bekannt. Jedoch wurde der Stoff nicht als eigenständiges Element erkannt. Erst 1751 konnte der schwedische Chemiker und Mineraloge Axel Frederic Cronstedt erstmalig Nickel in reiner Form darstellen. Da Cronstedt es aus Kupfernickel (Rotnickelkies, Nickelin) extrahierte, behielt er den Namen bei – und zog so gleichzeitig eine direkte Linie zur Etymologie des Mittelalters.
Nickel: Vorkommen und Herkunft
An der Erdhülle (= bis 16 km Tiefe) hat Nickel einen Masseanteil von 0,015 Prozent. Auf die Erdkruste bezogen (= bis 35 km Tiefe) liegt der Anteil jedoch nur bei 0,008 Prozent. Wissenschaftler gehen allerdings davon aus, dass der Erdkern (= ab 2.900 km Tiefe) zu 5,2 Prozent seiner Gesamtmasse aus dem Metall besteht. Hier liegt das Nickel in reiner (gediegener) Form vor:
- Im äußeren Erdkern flüssig,
- im inneren Kern fest – dieser besteht wahrscheinlich aus 20 % Nickel und 80 % Eisen.
In der Erdkruste sind gediegene Nickelvorkommen eher selten und finden sich an nur wenigen Stellen, die sich über den gesamten Globus verteilen. Deutlich häufiger findet sich Nickel in Mineralen gebunden. Auffallend oft handelt es sich um sulfidische Erzverbindungen, also solche, in denen eine Verbindung mit Schwefel besteht. Die wichtigsten Nickelminerale und ihr Nickelanteil:
- Chloanthit 28 %
- Garnierit 25-46 %
- Gersdorffit 35 %
- Millerit 65 %
- Pentlandit 10-45 %
- Rotnickelkies („Nickelin“) 44 %
Bekannt sind gut 200 Nickelminerale. Darunter finden sich auch solche, die einen deutlich höheren Anteil aufweisen, aber auf der Erde so selten vorkommen, dass ein Abbau nicht lohnt. Was die Förderung in Minen anbelangt, so verteilten sich die weltweiten Produktionsmengen 2021 folgendermaßen:
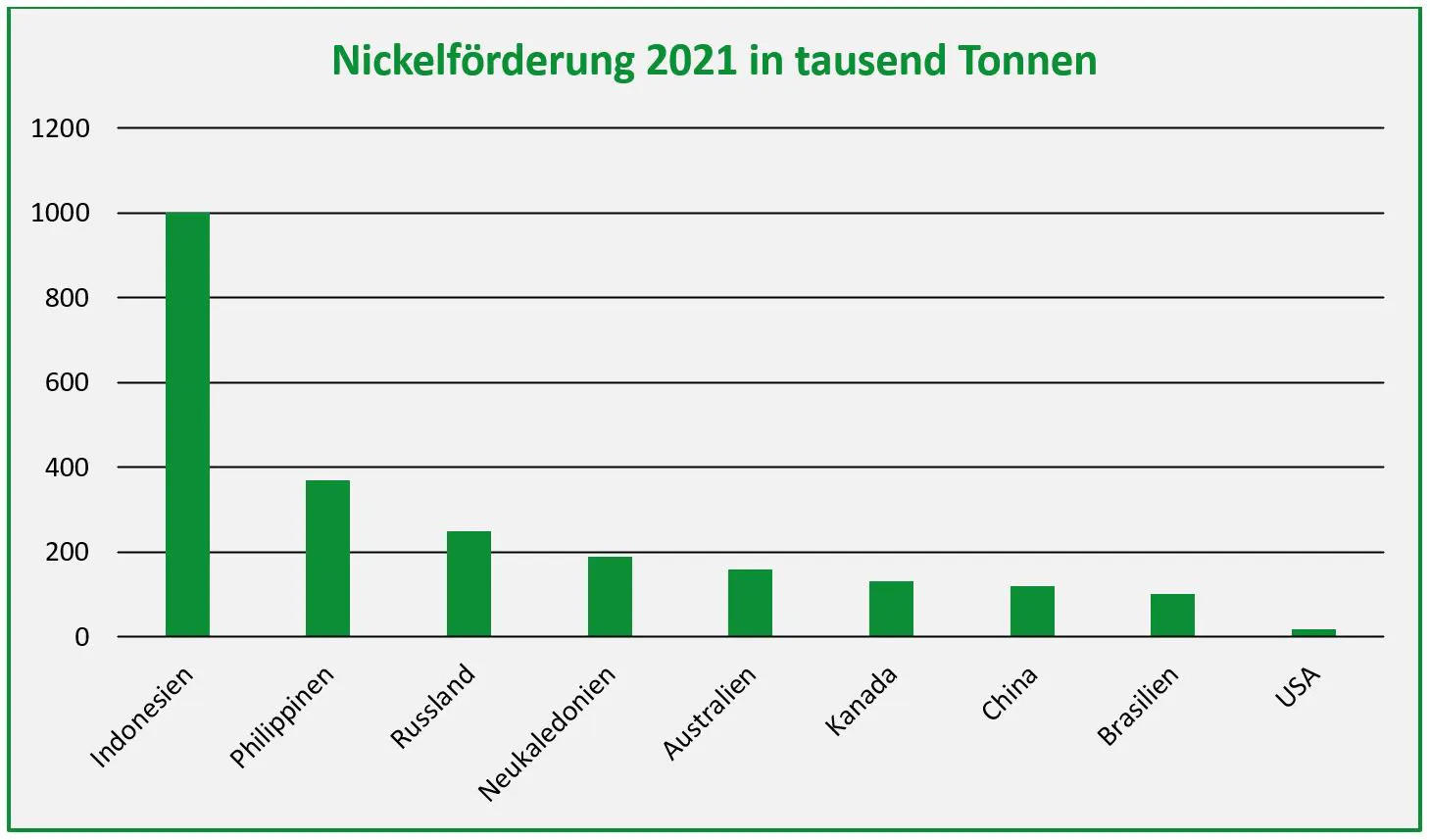
Die Gesamtfördermenge aller weiteren Staaten betrug im gleichen Zeitraum 410.000 Tonnen. Da die südpazifische Inselgruppe Neukaledonien zu Frankreich gehört, entfällt diese Produktion rechtlich auf die europäische Nation.
Nickel: Extraktions- und Herstellungsmethoden
Die geförderten Nickelerze sind naturgemäß zunächst unbrauchbar. Daher ist es nötig, den Erzen den Nickelgehalt zu entziehen. Der typische Prozess bei den meist Kupfer enthaltenden Erzen ist deutlich aufwendiger als bei Eisenerz. Er verläuft nach der groben Zerkleinerung in mehreren Schritten:
- Das Erz wird äußerst fein zermahlen und anschließend in dieser Form in einen Flotationsbehälter Dieser „Kessel“ ist mit einer Flüssigkeit (Suspension) gefüllt, die unter anderem Tenside und Schaumbildner enthält. Dieses Gemenge wird gerührt oder mit Luft angereichert. Es entsteht ein Schaum, an dem die metallhaltigen Bestandteile besser haften als das taube Gestein (Gangart). Auf der Oberfläche sammelt sich so allmählich ein Schaum aus deutlich konzentrierterem Nickelerz-Pulver.
- Das Pulver wird in Öfen geröstet. Darin enthaltenes Eisensulfid wird dabei in -oxid umgewandelt. Nach Hinzugabe von Koks und Silikaten entsteht eine Eisensilikat-Schlacke. Sie wird unter anderem als Mittel beim Sandstrahlen eingesetzt. Nach dem Abstich des Eisensilikats verbleibt sogenannter Kupfer-Nickel-Rohstein, der noch Eisensulfid enthält. Dies muss in einem weiteren Prozess in einem Konverter durch Einbringung von Sauerstoff und Siliziumdioxid zu Eisenoxid umgewandelt werden. Übrig bleibt Kupfer-Nickel-Feinstein, der zu 80 Prozent aus den beiden Elementen und im Rest aus Schwefel besteht.
- Der Kupfer-Nickel-Feinstein wird in einem Hochofen mit Natriumsulfid vermischt und aufgeschmolzen. Dabei trennt sich Nickelsulfid vom Kupfer ab. Dies muss danach erneut geröstet werden, wodurch das Nickelsulfid in -oxid umgewandelt wird. Nach erneuter Zugabe von Koks wird dieser Sauerstoffanteil reduziert und es verbleibt reines Nickel.
 Typischerweise ist dieses (Roh‑)Nickel nach wie vor ein Zwischenprodukt mit einem zu geringen Reinheitsgrad. Um Rein- und Reinstnickel zu gewinnen, wird das Rohnickel in einer elektrolytischen Nickelsalzlösung raffiniert.
Typischerweise ist dieses (Roh‑)Nickel nach wie vor ein Zwischenprodukt mit einem zu geringen Reinheitsgrad. Um Rein- und Reinstnickel zu gewinnen, wird das Rohnickel in einer elektrolytischen Nickelsalzlösung raffiniert.
Dazu wird es als Anode geschaltet, ein Blech aus Feinnickel dient als Kathode. Das Rohnickel und alle anderen Bestandteile lösen sich beim Elektrolyseprozess auf. Nur das reine Nickel wandert in Richtung Kathode. Es verbleibt ein Produkt mit etwa 99,90 Prozent Reinheit.
Sofern ein noch höherer Reinheitsgrad gewünscht ist, wird das Mond-Verfahren angewandt. Dabei wird das Reinnickel bei 80°C mit Kohlenmonoxid gespült. Dies entzieht gasförmiges Nickeltetracarbonyl. Wird dieses Gas in eine 180° C heiße Kammer mit Nickelkugeln geleitet, zersetzt sich das Nickeltetracarbonyl wieder zu Nickel und Kohlenmonoxid; ersteres mit 99,99 Prozent Reinheit.
Nickel: Verwendung in Stählen und anderen Metallen
Wie bereits erwähnt, wird das meiste geförderte Nickel in Stahlwerken eingesetzt. Der Grund liegt darin, weil Nickel durch seine physikalischen und chemischen Eigenschaften nicht nur gut mit dem Eisen harmoniert, sondern überdies auch mit einer ganzen Reihe von anderen Legierungselementen. Die wichtigsten Eigenschaften von Nickel für verschiedene Stähle:
- Erhöhung der Härte
- Erhöhung der Zähigkeit
- Erhöhung der Duktilität (Zugfestigkeit jenseits der Streckgrenze)
- Reduzierung der Korrosionsanfälligkeit (ab 8 % Anteil)
 Bei den meisten Eisenlegierungen ist Nickel jedoch nur ein wichtiges Legierungselement unter mehreren. Der bekannte, 1912 von Krupp erfundene, Edelstahl V2A etwa (1.4301) enthält nur 8 Prozent Nickel und 18 Prozent Chrom.
Bei den meisten Eisenlegierungen ist Nickel jedoch nur ein wichtiges Legierungselement unter mehreren. Der bekannte, 1912 von Krupp erfundene, Edelstahl V2A etwa (1.4301) enthält nur 8 Prozent Nickel und 18 Prozent Chrom.
Unter anderem dort, wo Systeme gegen Magnetfelder abgeschirmt werden müssen, kommen allerdings sehr spezielle Nickel-Eisen-Legierungen zum Einsatz, die bis zu 80 Prozent Nickel enthalten können. Entsprechende Bleche werden beispielsweise in den Gehäusen (mechanischer) Uhren genutzt, damit deren Gangstabilität nicht beeinflusst wird.
Aufgrund der hohen Stabilität bei hohen Umgebungstemperaturen und/oder in korrosiven Umgebungen finden Nickellegierungen auch Anwendung in zahlreichen anderen Bereichen – teils sogar unter völliger Abwesenheit von Eisen:
- Turbinenbauteile für die Luftfahrt und Kraftwerke
- Katalysatoren in der chemischen Industrie
- hochpräzise elektrische Widerstände („Konstantan“ aus 45 % Nickel und 55 % Kupfer)
- in manchen Bauarten von Brennstoffzellen
In Form des sogenannten austenitischen Gusseisens mit Kugelgraphit ist Nickel zudem an einem Gusseisen für extreme Sonderanwendungen beteiligt. Dadurch lassen sich Bauteile herstellen, die anderweitig nur unter Verwendung deutlich teurerer Edelstähle gefertigt werden können.
Unter anderem werden Zylinderlaufbuchsen in Verbrennungsmotoren daraus gefertigt. Ferner wird geprüft, künftige Generationen von Reaktordruckbehältern aus diesem Material zu fertigen – nachdem beispielsweise die „Castor“-Behälter für hochradioaktiven Atommüll schon seit langer Zeit daraus bestehen.
Nickel: Verwendung als reines Metall
Nickel ist zwar definitiv ein Legierungselement. Das bedeutet jedoch nicht, dass seine optischen und vor allem korrosionsschützenden Eigenschaften nicht für sich allein genutzt würden.
 Zwar sind die Anwendungsbereiche für reines Nickel deutlich kleiner, es gibt sie jedoch. Einer besonders langen Geschichte erfreut sich dabei die Praxis des Vernickelns. Meist läuft dieser Prozess ebenfalls in einem elektrolytischen Bad ab. Dabei wird auf elektrochemischem Weg reines Nickel auf eine andere leitende Oberfläche aufgebracht.
Zwar sind die Anwendungsbereiche für reines Nickel deutlich kleiner, es gibt sie jedoch. Einer besonders langen Geschichte erfreut sich dabei die Praxis des Vernickelns. Meist läuft dieser Prozess ebenfalls in einem elektrolytischen Bad ab. Dabei wird auf elektrochemischem Weg reines Nickel auf eine andere leitende Oberfläche aufgebracht.
Häufig handelt es sich dabei um Stähle, die selbst kein Nickel enthalten. Wahlweise, weil sie deshalb günstiger herzustellen sind oder weil der Stahl Eigenschaften aufweisen soll, die mit einer Nickellegierung nicht möglich wären. Daneben wird die Technik des Vernickelns häufig bei Aluminium-, Messing- und Zinkdruckgussprodukten angewendet.
Auch bei Schmuck und ähnlichen Gegenständen mit Hautkontakt werden Nickel oder vernickelte Produkte nicht zuletzt aufgrund der optischen Eigenschaften gerne genutzt. Hier kommt allerdings eine besondere Problematik dieses Elements zum Tragen:
Nickel und das Thema Unverträglichkeiten
So wichtig Nickel insgesamt für zahlreiche Produkte ist, so problematisch kann es sein, wenn es auf oder in den Körper gelangt. Vor allem Nickelverbindungen (metallisches Nickel ausgenommen) gelten beim Körperkontakt durch Einatmen als krebserzeugend. Deutlich relevanter, da häufiger, sind jedoch Probleme, die durch Hautkontakt hervorgerufen werden:
- Der stets auf der menschlichen Hautoberfläche vorhandene Schweiß hat leicht saure Eigenschaften (pH-Wert zirka 4,5).
- Dadurch können sich bei Gegenständen aus reinem Nickel oder solchen, die vernickelt sind, Nickelionen lösen. Sie können bei jedem Menschen die Hautbarriere durchdringen.
- Normalerweise ist Nickel als Spurenelement lebenswichtig. Ferner ist die Größe derartiger Nickelionen zu gering, um vom Körper erkannt zu werden.
- Allerdings können die Nickelionen aufgrund ihrer Eigenschaften eine Verbindung mit manchen körpereigenen Eiweißen eingehen. Dadurch werden sie sozusagen für das körpereigene Immunsystem sichtbar.
- Bei manchen Menschen wird beim Vorhandensein von Nickel-Eiweiß-Verbindungen eine Abwehrreaktion hervorgerufen; besonders außen auf der Haut. Dies äußert sich durch Rötungen, Brenn- und Juckreize und allgemein entzündliche Reaktionen (Ekzeme).
 Tatsächlich ist eine Nickelallergie die häufigste beobachtete Kontaktallergie bei Menschen. Tritt sie einmal auf, ist sie nicht mehr reversibel. Zwar heilen die betroffenen Hautpartien schon nach wenigen Tagen wieder ab. Jedoch besteht bei jedem erneuten Kontakt das Risiko für eine neue allergische Reaktion. Laut dem deutschen Allergie- und Asthmabund sind zehn bis zwölf Prozent der Bevölkerung davon betroffen. Besonders häufig leiden junge Frauen unter einer Nickelallergie.
Tatsächlich ist eine Nickelallergie die häufigste beobachtete Kontaktallergie bei Menschen. Tritt sie einmal auf, ist sie nicht mehr reversibel. Zwar heilen die betroffenen Hautpartien schon nach wenigen Tagen wieder ab. Jedoch besteht bei jedem erneuten Kontakt das Risiko für eine neue allergische Reaktion. Laut dem deutschen Allergie- und Asthmabund sind zehn bis zwölf Prozent der Bevölkerung davon betroffen. Besonders häufig leiden junge Frauen unter einer Nickelallergie.
Da sich die Zahlen in anderen Staaten ähnlich verhalten, gilt innerhalb der EU bereits seit 1994 die sogenannte Nickelrichtlinie. Demnach dürfen nickelhaltige Produkte, die durch ihre Eigenschaften für einen ständigen Hautkontakt vorgesehen sind, pro Quadratzentimeter Fläche und Woche nicht mehr als 0,5 µg Nickel freisetzen. Bei hautpenetrierendem Schmuck (etwa Ohrstecker und Piercings) liegt der Wert sogar bei nur 0,2 µg.
Bildquellen:
Bild 1: stock.adobe.com © Negro Elkha
Bild 2: stock.adobe.com © evgenii_v
Bild 3: stock.adobe.com © Björn Wylezich
Bild 4: stock.adobe.com © Bildwerk
Bild 5: stock.adobe.com © Victor Koldunov
Bild 6: stock.adobe.com © ErdalIslak



